
Cos’è emerso dai dati raccolti nell’ambito della sorveglianza sulla sicurezza dei vaccini anti COVID-19 in un anno di somministrazioni? Scopriamolo insieme. Intro.
Lo scorso 9 febbraio 2022, tramite un comunicato stampa, l’AIFA – Agenzia italiana del farmaco – ha pubblicato un nuovo rapporto sulla sicurezza dei vaccini anti COVID-19, facendo il punto di quanto accaduto in un anno esatto di somministrazioni.
Infatti, la campagna vaccinale nel nostro Paese ha avuto inizio il 27 dicembre 2020, con il Vaccine Day. Da quel giorno sono state somministrate più di 100 milioni di dosi dei 4 vaccini approvati e disponibili in Italia.
Cos’è successo in questo anno di vaccinazioni? Vediamo insieme cosa emerge dal rapporto annuale sulla sicurezza dei vaccini anti COVID-19 pubblicato da AIFA (lo trovi qui).
Indice dei Contenuti
Un anno di vaccinazione: i dati raccolti
Il rapporto annuale redatto da AIFA si riferisce al periodo compreso tra il 27 dicembre 2020 e il 26 dicembre 2021, raccogliendo i dati relativi quindi a un anno esatto di somministrazione.
In questi 12 mesi sono state somministrate 108.530.987 dosi di vaccino, con un tasso di segnalazione di 109 ogni 100.000 dosi somministrate, pari in totale a 117.920.
Ricordiamo che, ad oggi, e durante il periodo di riferimento, i vaccini disponibili e impiegati nella campagna vaccinale italiana sono quattro:
- Comirnaty (Pfizer/BioNTech), vaccino a mRNA autorizzato dal 22/12/2020 e utilizzato dal 27/12/2020;
- Spikevax (Moderna), vaccino a mRNA autorizzato dal 07/01/2021 e utilizzato dal 14/01/2021;
- Vaxzevria (AstraZeneca), vaccino a vettore virale ricombinante autorizzato dal 29/01/2021 e utilizzato dal 01/02/2021;
- COVID-19 Vaccino Janssen (Janssen Cilag), vaccino a vettore virale autorizzato dal 12/03/2021 e utilizzato dal 22/04/2021.
Com’è noto a tutti, nel corso dei mesi i vaccini ex AstraZeneca e Janssen sono stati impiegati sempre meno, virando sui due prodotti basati sulla tecnologia a mRNA.
Comirnaty è stato il vaccino più utilizzato (69,1%), seguito da Spikevax (18,3%), Vaxzevria (11,2%) e COVID-19 Vaccino Janssen (1,4%).
Le segnalazioni per tipologia di vaccino sono invece così distribuite:
- Comirnaty 68%;
- Vaxzevria 19,8%;
- Spikevax 10,8%;
- COVID-19 vaccino Janssen 1,4%.

Le segnalazioni di eventi avversi
Come indicato, nei 12 mesi analizzati sono state registrate 117.947 segnalazioni di eventi avversi su un totale di 108.530.987 dosi dei vaccini, con un tasso di segnalazione pari a 109 su 100.000.
L’età media delle persone che hanno avuto un evento avverso è 47,2 anni (età mediana di 47 anni).

Il tasso di segnalazione è maggiore nelle fasce di età comprese tra i 20 e i 60 anni, per poi diminuire nelle fasce d’età più avanzate e nei giovanissimi, con un tasso di segnalazione mediamente inferiore dopo la 2a dose e ancora più basso dopo la 3a dose.
A fronte di un’esposizione sovrapponibile fra i sessi (52% delle dosi somministrate nel sesso femminile e del 48% nel sesso maschile), il 70% delle segnalazioni riguarda le donne (148/100.000 dosi somministrate) e il 29% gli uomini (65/100.000 dosi somministrate), indipendentemente dal vaccino e dalla dose somministrata.

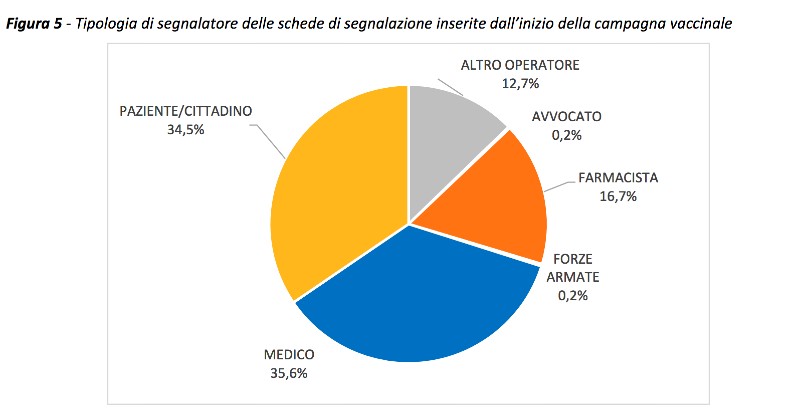
Circa il 65% delle segnalazioni proviene da operatori sanitari, prevalentemente medici e farmacisti, mentre il 34,5% da pazienti/cittadini, con un modesto incremento rispetto ai mesi precedenti. Il 94,8% circa di queste segnalazioni è di tipo spontaneo mentre la rimanente è ascrivibile a studi di farmacovigilanza attiva.
Indipendentemente dal vaccino, dalla dose e dalla tipologia di evento, la reazione si è verificata nella maggior parte dei casi (73% circa) nella stessa giornata della vaccinazione o il giorno successivo, e solo più raramente l’evento si è verificato oltre le 48 ore successive.

Gravità delle segnalazioni
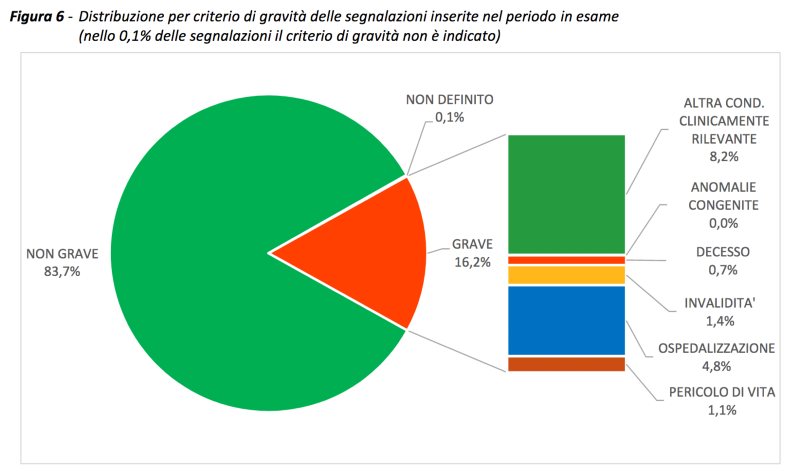
L’83,7% delle segnalazioni è riferita a eventi non gravi, con un tasso di segnalazione pari a 91/100.000 dosi somministrate, mentre il restante il 16,2% a eventi avversi gravi (la gravità non è riportata nello 0,1% delle segnalazioni, n. 148).
- il 77% circa delle segnalazioni non gravi riporta come esito “risoluzione completa” (guarigione) o “miglioramento” già al momento della segnalazione;
- il 50% circa delle segnalazioni gravi riporta come esito la “risoluzione completa” o il “miglioramento” dell’evento;
- il 32% delle segnalazioni gravi risulta non ancora guarito al momento della segnalazione.

Il nesso di causalità secondo l’algoritmo del WHO è stato inserito in circa l’83% delle segnalazioni di eventi avversi gravi ed è risultato correlabile alla vaccinazione nel 35,9% di tutte le segnalazioni gravi valutate, indeterminato nel 37,7% e non correlabile nel 21,6%.
Decessi
Per quanto riguarda i decessi, al 26/12/2021 nella RNF (Rete Nazionale di Farmacovigilanza) sono state inserite complessivamente 758 segnalazioni gravi che riportano l’esito “decesso”, ovvero 0,7 eventi con esito fatale segnalati ogni 100.000 dosi somministrate.

- il 46,4% dei casi riguarda donne, il 52,6% uomini, mentre lo 0,9% non riporta questo dato;
- l’età media è di 79 anni;
- in 456 casi il decesso è segnalato dopo la prima dose, in 267 dopo la seconda e in 35 dopo la terza;
- il 76,5% delle segnalazioni con esito decesso presenta una valutazione del nesso di causalità con l’algoritmo del WHO, in base al quale:
- il 57,9% dei casi risulta non correlabile;
- il 30,2% risulta indeterminato;
- l’8,1% risulta inclassificabile per mancanza di informazioni sufficienti.
- Il rimanente 23,5% è in attesa di ulteriori informazioni necessarie alla valutazione del nesso di causalità.
Quindi, complessivamente, sui 580 decessi valutati sono risultati correlabili alla vaccinazione solo 22, il 3,8%, pari a circa 0,2 casi ogni milione di dosi somministrate.
Gli eventi avversi segnalati
Come riportato nel comunicato stampa dell’AIFA, nel quale si riassumono le evidenze raccolte con il rapporto annuale, per tutti i vaccini gli eventi avversi più segnalati, perlopiù non gravi e già risolti al momento della segnalazione, sono:
- febbre;
- stanchezza;
- cefalea;
- dolori muscolari/articolari;
- dolore in sede di iniezione;
- brividi;
- nausea.
Entrando più nel dettaglio, vediamo quali sono stati gli eventi avversi più segnalati in base al tipo di vaccino somministrato.





Il 70,9% delle segnalazioni riguarda le donne e il 28,5% gli uomini, indipendentemente dal vaccino e dalla dose somministrata (il sesso non è riportato nello 0,6% delle segnalazioni).
L’età media delle persone che hanno riportato un evento avverso dopo la somministrazione della terza dose è pari a 50,7 anni (età mediana di 50 anni).

Per quanto riguarda, invece, la vaccinazione eterologa, ovvero la somministrazione di un vaccino differente rispetto a quello ricevuto per la prima dose, o per le prime due in caso di dose booster, la maggior parte delle segnalazioni sono relative alla somministrazione di un vaccino a mRNA dopo prima somministrazione di un vaccino a vettore adenovirale, per lo più sono non gravi e presentano le stesse caratteristiche del resto delle segnalazioni.
Vaccinazioni in età pediatrica
La vaccinazione anti COVID-19 in età pediatrica è stata autorizzata dalle varie autorità regolatorie internazionali in due fasi differenti. La prima ha riguardato i soggetti dai 12 ai 17 anni, mentre la seconda quelli dai 5 agli 11 anni.
In Italia le vaccinazioni anti-COVID-19 in età pediatrica sono state avviate a partire da giugno 2021 nella fascia di età 12-15 anni, mentre il 1° dicembre 2021 è stata approvata anche la formulazione pediatrica per la fascia d’età 5-11 anni.
I vaccini approvati a tale scopo e impiegati in Italia sono stati i due a mRNA, ovvero Comirnaty (con l’87,5% delle somministrazioni) e Spikevax (con il 12,5% delle somministrazioni), nelle seguenti modalità:
- Vaccino Comirnaty:
- ciclo primario vaccinale (prima e seconda dose) a partire dai 12 anni; ogni dose (0,3 mL) contiene 30 microgrammi di principio attivo;
- dose booster (terza dose, 0,3 mL) ai soggetti della fascia di età 12-15 anni con elevata fragilità motivata da patologie concomitanti/preesistenti e agli appartenenti alla fascia di età 16-17 anni;
- Vaccino Comirnaty (formulazione pediatrica): autorizzato nella fascia 5-11 anni; ogni dose (0,2 mL) contiene 10 microgrammi di principio attivo;
- Vaccino Spikevax: a partire dai 12 anni di età; ogni dose (0,5 mL) contiene 100 microgrammi di RNA messaggero (mRNA).
Al 26 dicembre 2021 risultano somministrate 4.178.361 di dosi di vaccino, il 96% delle quali nella fascia di età 12-16 anni (4.005.471 dosi) e il 4% nella fascia 5-11 anni (172.890 dosi), e sono state registrate complessivamente 1.170 segnalazioni di sospette reazioni avverse manifestatesi nella popolazione pediatrica, che rappresentano l’1% di tutte le segnalazioni, con un tasso di segnalazione pari a 28 eventi ogni 100.000 dosi somministrate nella fascia pediatrica.
Si tratta di un dato inferiore rispetto a quello riscontrato nella popolazione generale (109 eventi ogni 100.000 dosi somministrate).
Nella popolazione pediatrica gli eventi avversi più frequentemente segnalati sono febbre, cefalea, stanchezza e vomito. Il 69% delle reazioni si sono risolte completamente o erano in miglioramento al momento della segnalazione.
I tassi di segnalazione nella fascia d’età 5-11 sono preliminari e al momento non emergono particolari problemi di sicurezza.
Vaccinazione in gravidanza e allattamento
La vaccinazione anti COVID-19 in gravidanza e allattamento ha avuto un avvio ritardato rispetto alla campagna vaccinale nel nostro Paese. Solo a fine settembre l’ISS, su sollecitazione delle varie associazioni di categoria, ha aggiornato le indicazioni sulla somministrazione dei vaccini alle donne incinta o in allattamento.
Come si legge nel comunicato stampa AIFA, la vaccinazione per COVID-19 è indicata sia in gravidanza sia in allattamento e non emergono particolari problemi di sicurezza dai dati di farmacovigilanza e di studi ad hoc in questa popolazione.
Non vi sono inoltre evidenze che suggeriscano che i vaccini anti-COVID-19 possano influenzare negativamente la fertilità in entrambi i sessi.
Nel rapporto integrale è dedicata una parte proprio a questo aspetto, con i risultati di alcuni studi condotti negli ultimi mesi sulla popolazione femminile, oltre a un approfondimento su anafilassi, sindrome di Guillain-Barré, miocarditi/pericarditi, paralisi di Bell e trombosi trombocitopenica.
Invitiamo a consultare il documento per tutti i dettagli.
